原創 潘文志 周達新 中山醫院上海心臟中心
心臟瓣膜病是一類常見的心臟疾病,隨著人口老年化,其逐漸成為繼高血壓、冠心病之后第三常見的心臟疾病。心臟瓣膜病的特點是癥狀明顯(胸悶氣促)、體征典型(聽診可聞及雜音)、診斷容易(心臟超聲即可以確診)。嚴重的心臟瓣膜病可明顯影響患者的壽命,預后較差。葛均波院士曾論斷“心臟瓣膜疾病是人類長壽征途上的需要跨越一道坎”()。由于是解剖形態學的改變,故心臟瓣膜病一般情況下藥物治療無法根治,需要采用機械物理方式才能徹底治療。既往,外科開胸手術是瓣膜病的標準治療手段。但近年來,隨著醫學技術的發展,心臟瓣膜病也可以通過介入(或稱經導管、經皮、經血管)方式進行有效治療。本文對心臟瓣膜介入治療的技術原理、歷史沿革和當前認識作簡要而系統的介紹。
一、技術分類及原理
總體而言,心臟瓣膜的手術治療可分為采用傳統的胸骨正中切口手術(1.0時代),微創外科(小切口)瓣膜手術(2.0時代),經導管瓣膜介入治療(3.0時代)。其中,微創外科瓣膜手術采用小切口、非胸骨全部劈開方式以減小手術創傷,通過電視胸腔鏡和外科手術機器人輔助進行手術。微創外科瓣膜手術雖然傷口小,但術中心臟仍要停跳、仍需要體外循環輔助。研究顯示,其雖然能降低手術創傷,但并不能降低手術風險。
心臟瓣膜介入治療的基本原理是采用導管介入方式,將治療器械壓縮到一個很細的導管(直徑4-10mm),然后穿刺外周血管(通常是股動脈或股靜脈)或者心前區,插入導管,并將器械輸送到所要治療瓣膜的位置,在超聲或者X線透視指導下,對瓣膜進行修復或者更換,從而達到治療目的。心臟瓣膜介入治療傷口較微創外科手術進一步縮小,且是在心臟跳動情況下進行手術二尖瓣狹窄最早出現的癥狀,無需心臟停跳及體外循環,避免這兩者引發的不良反應,故手術安全性明顯提高。
目前心臟瓣膜介入治療按照原理可以分為三類:①球囊擴張術,采用一個可膨脹的球囊,通過導管輸送到狹窄的瓣膜進行擴張,撕開瓣葉在交界處的粘連而不損傷瓣葉,因此可以治療狹窄卻不導致瓣膜反流。代表技術為經皮二尖瓣球囊擴張及經皮肺動脈瓣球囊擴張;②經導管瓣膜置換術。其原理是將一個三葉的生物瓣縫合在一大金屬支架上構成了介入瓣膜,然后將該介入瓣膜壓縮到輸送導管,將之放置在病變的瓣膜處,套在病變的瓣膜里,從而實現對原先病變的瓣膜的功能替代;③經導管瓣膜修復術,是基于外科手術的基本術式的原理,采用特殊的可壓縮器械,經導管輸送到病變的瓣膜位置,對瓣膜進行形態結構修復,主要包括瓣葉修復,瓣環環縮及人工腱索植入等技術。
二、經皮球囊擴張成形術
經皮二尖瓣球囊擴張(PBMV):
歷史沿革:
1902年Cutler與Levine首先經左心室心尖部插入特制彎刀切開二尖瓣交界處治療二尖瓣狹窄。1925年Souttar經左心耳途徑用手指分離擴大二尖瓣瓣口。1954~1960年Beck、Glenn、Logan、Turner、Tubbs等先后研制二尖瓣機械擴張器,經左心耳或經心尖插入瓣膜區,在左心房內手指的指引下擴大瓣口,提高治療效果。以上的術式均在心臟跳動、未打開的情況下,根據手指觸摸手感進行二尖瓣交界處的分離,故也稱之為二尖瓣閉式分離。1976年日本醫生Inoue(井上寬治)等設計出由兩層乳膠夾一層尼龍網而成的、具有自身定位能力的二尖瓣球囊導管,稱為Inoue球囊導管,將球囊導管沿股靜脈、右心房并經房間隔穿刺送至狹窄的二尖瓣口,然后充盈球囊使狹窄的二尖瓣口擴張成形(圖1), 并于1984年進行首次臨床報道,之后該器械成為PBMV的全世界標準器械,延用至今。
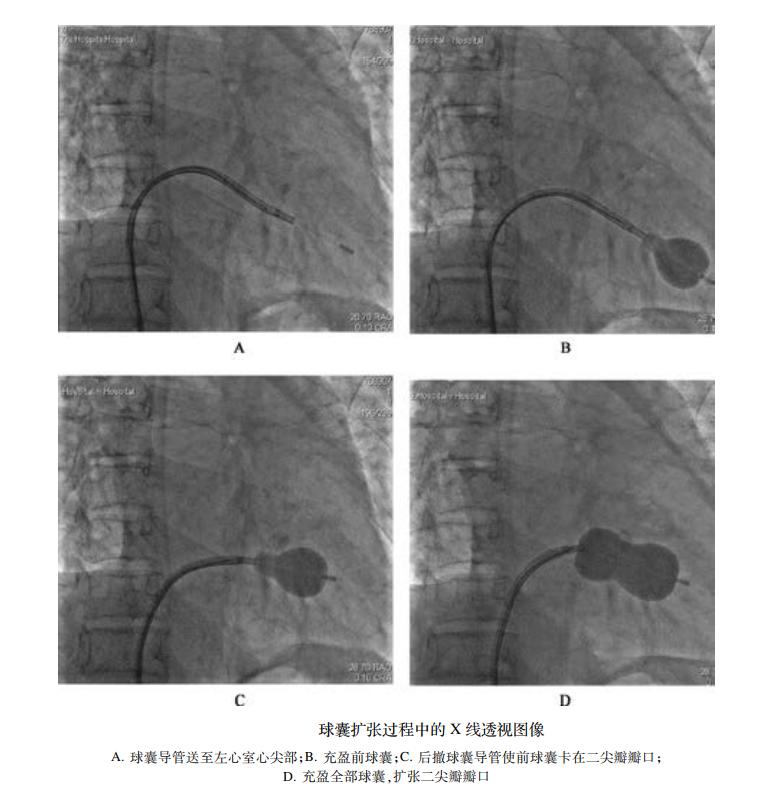
圖1. PBMV 手術的操作過程
當前認識:
大量研究結果顯示,PBMV即刻可產生血流動力學改善,二尖瓣瓣口面積增加,跨瓣壓、左心房壓及肺動脈壓下降,心排血量增加,生活質量提高。由于效果確切,微創安全,歐美及我國指南都將PBMV推薦為解剖合適的風濕性二尖瓣狹窄患者首選的治療選擇(I 類指證,A類證據)。風濕性二尖瓣狹窄在西方很少見,在我國仍常見,因此我國在這方面積累了豐富經驗。表1是我國2016年PBMV指南中PBMV的適應證。PBMV的主要局限性在于有一定再狹窄率,5年再狹窄率約為15%,10年再狹窄率約為25%,年輕患者(小于50歲)再狹窄率更低些。但再狹窄后仍可再行PBMV治療,從而延緩外科手術的時機。

表1 我國2016年PBMV指南中PBMV的適應證
經皮肺動脈瓣球囊擴張(PBPV)
1982年,Kan首先報道采用球囊擴張技術治療先天性肺動脈瓣狹窄(PS),這種技術被稱為經皮球囊肺動脈瓣成形術(PBPV),其因簡便、有效、安全而得到廣泛應用。隨著現代工業和導管技術的發展,大量關于PBPV的臨床應用研究被進行,這些研究結果證實PBPV可為大部分PS患者的首選治療手段,可替代外科開胸手術,成為各大指南首選推薦的治療手段(I 類指征)。2020年ESC先心指南推薦的PS進行PBPV手術主要指征為(具有以下之一):出現相關癥狀,峰值跨瓣壓差大于64mmHg,右心室功能下降三尖瓣反流,合并右向左分流。
三、經導管主動脈瓣置換術(TAVR)
歷史沿革:
1965年,Hywel Davies設計了一種降落傘樣的瓣膜安裝在導管上,經股動脈送至降主動脈,動物實驗顯示其對主動脈關閉不全狗有血流動力學益處(圖2)。隨后有類似幾種瓣膜模型用于主動脈關閉不全動物的實驗。1992年Anderson把豬的瓣膜縫合在一個不銹鋼網狀支架上模型進行瓣膜置入手術均獲得成功,但有部分動物出現冠脈阻塞而死亡(圖3)。Cribier等2001年報道了一種可以經導管置入的人工主動脈瓣支架,由球囊膨脹型不銹鋼支架和牛心包制成的瓣葉組成,在體外血流動力學測試以及短期的動物實驗中均顯示了良好的血流動力學性能。2002年Cribier等完成了第一例人體TAVR,書寫了經導管介入瓣膜置換治療的新篇章,該系列的瓣膜即為愛德華公司球囊擴張式瓣膜Sapien(圖4)。2005年12月Grube等首次使用自膨脹式的瓣膜完成TAVR術,該系列瓣膜以美敦力的CorevValve瓣膜系列為代表。類似的,目前國內臨床應用的主要為自膨脹式瓣膜
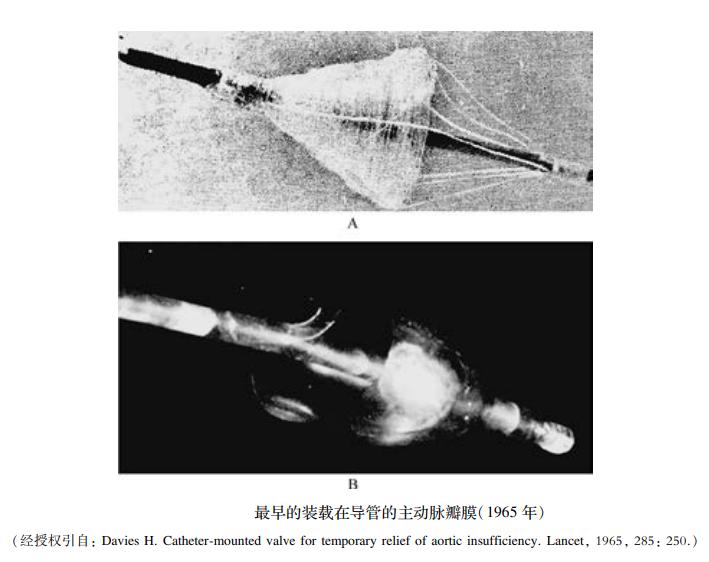
圖2. 最早的經導管主動脈瓣瓣膜樣品
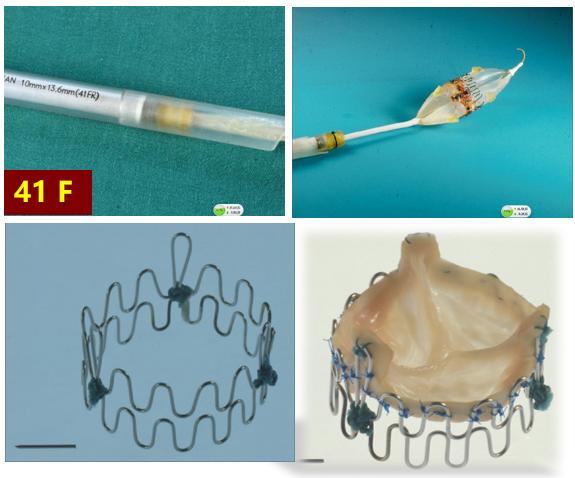
圖3. Anderson 用于動物試驗的TAVR瓣膜樣品

圖4. 愛德華公司的球囊擴張瓣膜系列
當前認識:
經過20年的發展, TAVR的器械經過數次迭代,目前性能已大大提高,具有小尺寸(輸送系統由最初的26F降低為目前最低14F)、防瓣周漏、可回收、可重新定位、自動錨定等等功能,因此TAVR的安全性已大大提高。TAVR已成為了近20年來心血管介入領域最閃耀的新星。大量高質量的RCT臨床研究(僅《新英格蘭醫學雜志》就累計發表10余篇TAVR相關的研究)證實TAVR的安全性及有效性。TAVR的適應證已從外科手術禁忌患者發展到外科手術高危患者、中危患者,目前對于高齡(65歲以上)、外科手術低危患者,指南也推薦行TAVR術(I類或II A類指征)。全球TAVR應用已超過50萬例。TAVR的基本原理是狹窄的主動脈瓣,通常很堅硬且構成了一個狹窄管道,該解剖特點可以為TAVR瓣膜的金屬支架提供良好的支撐固定作用。起初,TAVR只用于三葉式的主動脈瓣狹窄患者,但隨著研究進展,發現對于二葉式主動脈瓣狹窄患者,TAVR人也是適用的,目前已受到指南推薦。隨著器械的改進,目前部位TAVR器械帶有錨定功能,因此,部分的解剖合適的主動脈瓣反流的患者也可以使用TAVR治療。由于TAVR植入的瓣膜是生物瓣,目前研究顯示其預期使用壽命為10-15年。然而,對于TAVR瓣膜達到使用壽命后出現瓣膜衰敗患者,可以在原先TAVR瓣膜內再植入一個TAVR瓣膜進行治療,緩解患者后顧之憂,但再次植入瓣膜的次數是有限的,因此對于年輕患者一般不建議植入TAVR瓣膜
四、經導管緣對緣修復(TEER)
歷史沿革:
TEER技術是一項基于外科二尖瓣緣對緣修復術的經導管介入技術,其采用二尖瓣夾合裝置(一個可壓縮、機械傳動的夾子),經股靜脈或心尖途徑植入,在超聲及X線引導下夾住二尖瓣反流區的前、后瓣葉并使之接合,使心臟收縮期時瓣葉之間間歇減少或消失,而舒張期時瓣口變成雙孔或多孔,從而達到減少或消除二尖瓣反流的效果。TEER是基于外科緣對緣修復的醫學原理,該術式由20世紀90年代由意大利外科醫生Otavio Alfieri首創。1991年,他為一名患者實施房間隔缺損外科修復手術術中打開心臟后發現該患者二尖瓣是雙孔型的,他發現這樣的二尖瓣在功能上也正常,且經過隨訪,該患者仍可長期健康的存活。受此病例啟發,他對一些二尖瓣反流患者手術時,把一些病變的二尖瓣瓣葉和對側的二尖瓣葉縫合在一起,形成雙孔二尖瓣,經過隨訪研究發現瓣膜功能也可長期保持正常。在外科緣對緣二尖瓣修復術的啟發下,人們開始開發各種各樣的TEER器械。Morales在1999年首先運用一種無需體外循環的二尖瓣緣對緣修復裝置。2002年Alfieri接著報道了一種經穿刺主動脈實施的二尖瓣緣對緣縫合裝置的動物實驗結果。 經靜脈穿房間隔實施的二尖瓣緣對緣縫合裝置Mobius(Edwards Lifesciences,Irvine,California)隨后在動物試驗中被證明安全有效。以上各種裝置由于設計上或技術上的缺陷最終未能廣泛運用于臨床,直到雅培公司MitraClip系統的出現,TEER裝置才真正走向臨床。該裝置采用經股靜脈-房間隔的路徑,輸送系統為24F(圖6)。2003年人們報道了成功使用MitraClip系統的動物實驗。同年,世界上第一例使用MitraClip系統行經導管二尖瓣修復術的人體手術亦取得成功。2018年,我團隊發明的世界首個經心尖TEER器械ValveClamp成功應用于臨床。
當前認識:
TEER技術的發展要比TAVR緩慢而崎嶇,原因在于無論是器械的研發還是手術操作都更復雜。隨著器械的改進以及臨床經驗積累,TEER已從開發研究變成臨床廣泛應用,目前全世界應用已超過15萬例。歐美指南已將TEER列為外科手術高危、解剖合適的二尖瓣反流患者的適應證(II A類指征)。TEER是基于外科緣對緣修復技術,或多或少的會導致瓣口面積減少,雖然這種瓣口面積減少通常不導致心臟功能的異常,但對某些術前瓣口面積不大患者顯然是不合適的。對于反流面積很大患者,也不可能使用多個夾子將二尖瓣廣泛夾合,因為這樣也會導致瓣口狹窄。對于交界區病變,該區域瓣葉較短,腱索較多,行TEER術難度較大。因此,相對于TAVR技術,目前的TEER技術對患者瓣膜的解剖條件要求更嚴格:從解剖學上將,絕大部分的主動脈瓣狹窄患者都能做TAVR;而對于TEERT手術,只有部分患者適合手術。其解剖要求主要為:返流束不能在交界區,瓣葉長度不能過短(短于6mm),術前瓣口面積不能太小(大于3.5cm2),反流區不能太寬泛(大于20mm)。雖然缺乏足夠多的長期隨訪數據二尖瓣狹窄最早出現的癥狀,然而,相對于TAVR手術,TEER手術具有更高的安全性,在解剖合適人群短中期效果時肯定。因此,對于解剖合適的外科手術高危者,不失為一種較好的治療手段。
總結及展望
心臟瓣膜病是一種常見的心臟疾病,明顯的影響著人類社會的健康。人類疾病治療技術的發展存在著普遍規律,通常都經歷了從無可為到有可為、從大創傷到小創傷甚至無創傷的過程。同樣,心臟瓣膜病先后經歷了最早的無法治療、傳統的胸骨正中切口手術(1.0時代)以及微創(小切口)手術(2.0時代),目前已經迎來了介入治療時代(3.0時代)。本文對主要幾個技術發展的歷史沿革進行梳理,我們可以發現每個成功應用于臨床的技術和器械,都是建立在前人大量探索研究基礎上的,都是“站在巨人肩膀上”才獲得成功。目前PBMV、PBPV、TAVR及TEER(MitraClip)技術已在全世界廣泛應用,得到普遍認可,而其他十余種心臟介入治療技術也在發展中,涵蓋了的三尖瓣、肺動脈瓣病變。雖然目前心臟瓣膜治療已進入3.0時代,但不是所有患者都適合行介入治療,前文提及的心臟瓣膜治療的3種手術方式在目前的臨床實踐中仍然并存。對于不同人群,適合的手術方式不盡相同。在未來的一段時間內,3種手術方式將既共存互補,又相互競爭。然而,毫無疑問的是,心臟瓣膜介入治療將是未來心臟瓣膜治療最重要的發展方向。
 名師輔導
環球網校
建工網校
會計網校
新東方
醫學教育
中小學學歷
名師輔導
環球網校
建工網校
會計網校
新東方
醫學教育
中小學學歷